Restaurer le microbiote en hémato-oncologie :
Les thérapies de MaaT Pharma pour le traitement de la maladie aigüe du greffon contre l’hôte (aGVH) et la prévention des complications de la greffe de cellules souches hématopoïétiques allogéniques (allo-GCSH) ont pour but de restaurer les fonctions physiologiques d’un microbiote sain afin de corriger les effets de facteurs de stress comme les antibiotiques et les chimiothérapies.
Restaurer et moduler le microbiote en immuno-oncologie :
Les thérapies de MaaT Pharma pour le traitement des tumeurs solides ont pour objectif de restaurer et moduler le microbiote , dans le but d’améliorer la réponse aux inhibiteurs de points de contrôle immunitaires, traitements souvent incontournables dans ces indications.
La maladie aiguë du greffon contre l’hôte (aGvH) survient chez les patients dans les 100 jours après une greffe de cellules souches ou de moelle osseuse. Les cellules greffées « attaquent » le receveur, provoquant une inflammation de la peau, du foie et/ou du tractus gastro-intestinal et entraînant une morbidité et une mortalité élevées. L’atteinte gastro-intestinale notamment est associée à des complications graves telles que diarrhées intenses, douleurs abdominales, hémorragies intestinales et mettant en jeu le pronostic vital du patient, avec un risque de mortalité accru, en raison des difficultés liées à la prise en charge d’une inflammation gastro-intestinale sévère et des risques associés d’infection, de malnutrition et de défaillance d’organes.
des patients recevant une allo-GCSH développent une aGvH.
Taux de mortalité constaté après 1 an chez les patients avec une aGvH cortico-résistante.
cas d’aGvH en 2018 aux USA, UK, France, Allemagne, Italie, Espagne et Japon.
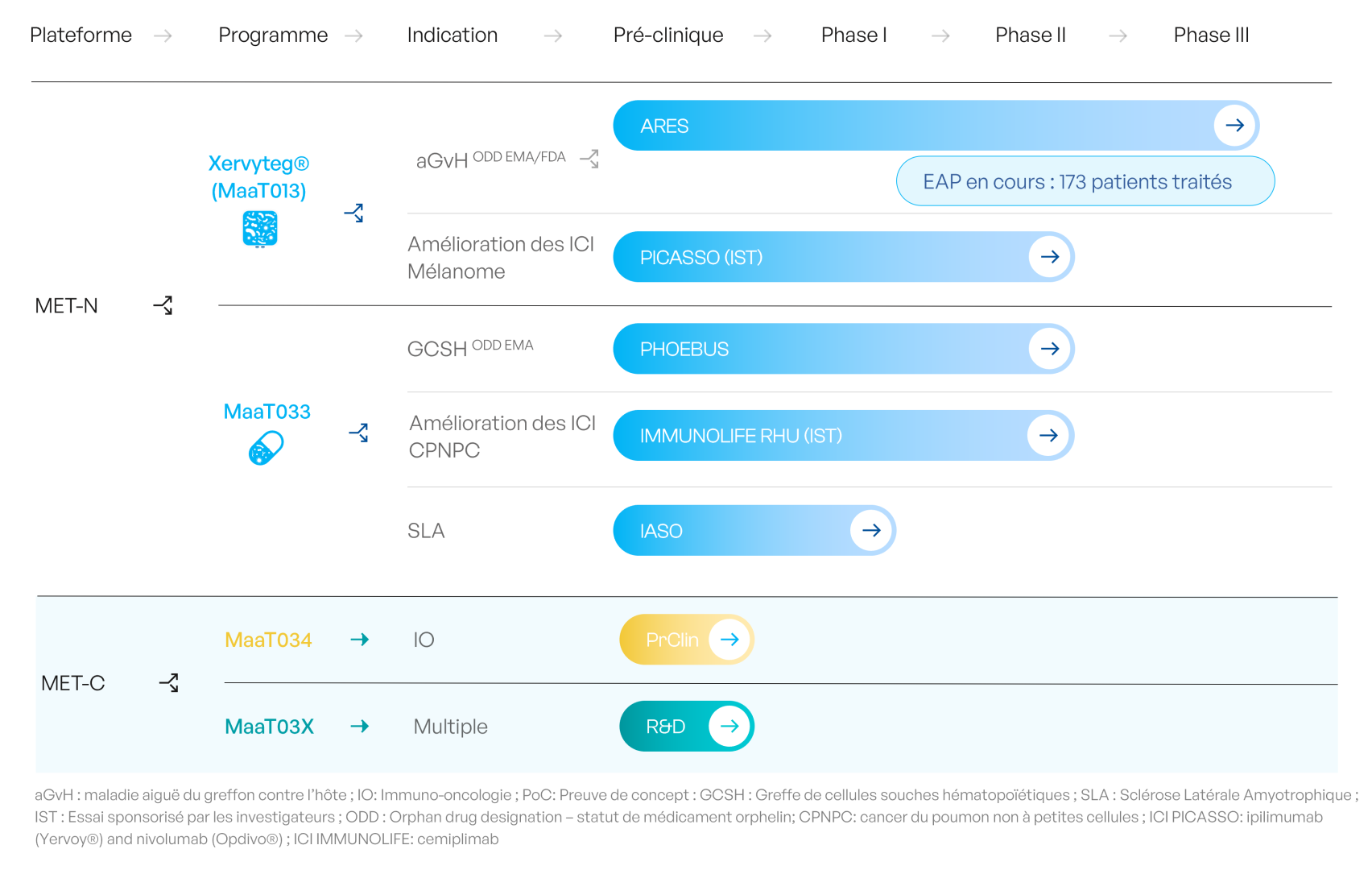
Xervyteg® (MaaT013) est une thérapie à écosystème complet (MET) dérivée de donneurs sains, standardisée, à haute richesse et haute diversité bactériennes , qui contient le ButycoreTM , un groupe de bactéries connues pour produire des acides gras à chaîne courte aux propriétés anti-inflammatoires. Xervyteg® (MaaT013) a obtenu la désignation de médicament orphelin de la part de la FDA et de l’EMA.

Xervyteg® (MaaT013) est un candidat-médicament issu du microbiote actuellement en cours d’examen réglementaire en Europe pour le traitement de la maladie aiguë du greffon contre l’hôte avec atteinte gastro-intestinale (GI-aGvH). Ce traitement a été évalué dans le cadre de l’essai clinique pivotal ARES (NCT04769895), le premier essai pivotal mondial portant sur une thérapie issue du microbiote en hémato-oncologie.
L’essai ARES a recruté en Europe 66 patients atteints de GI-aGvH réfractaire aux traitements de première ligne par corticoïdes et de deuxième ligne par ruxolitinib, les standards actuels de prise en charge.
Étapes cliniques majeures :
– Premier patient traité dans l’essai clinique pivotal ARES
– Avis positif suite à l’évaluation du DSMB* pour l’essai pivotal en cours, confirmant le profil de sécurité
– Résultats principaux positifs de l’étude pivotale ARES évaluant MaaT013 dans la maladie aiguë du greffon contre l’hôte, montrant une forte efficacité et un profil de sécurité favorable
– Conclusion positive de l’examen final du DSMB pour l’essai clinique pivotal, confirmant un profil bénéfice-risque favorable
– Dossier de demande d’autorisation de mise sur le marché (AMM) soumis à l’Agence européenne des médicaments (EMA) en juin 2025 pour le traitement de la GI-aGvH
La transplantation de cellules souches hématopoïétiques allogéniques (allo-GCSH) est une procédure susceptible de sauver la vie de patients souffrant de cancers du sang comme la leucémie aigüe myéloïde. Malheureusement, elle peut également être associée à des complications graves, comme des infections, la maladie du greffon contre l’hôte, ou la neutropénie, qui contribuent à une mortalité de l’ordre de 34%6, un an après la procédure chez les patients de plus de 50 ans.

Le mode d’action supposé de MaaT033 est immuno-modulateur :
Des résultats positifs de Phase 1b
En juin 2022, MaaT Pharma a annoncé des résultats positifs pour MaaT033 dans un essai clinique de Phase 1 (CIMON) auprès de patients atteints de leucémie myéloïde aiguë, à savoir une bonne implantation des espèces bactériennes bénéfiques, qui se maintient dans le temps, associée à un profil de sécurité satisfaisant.
Plus d’informations :
Essai clinique de Phase 2b en cours
En novembre 2023, MaaT Pharma a annoncé le traitement du premier patient dans le cadre de son essai de Phase 2b (PHOEBUS) évaluant l’efficacité de MaaT033 dans l’amélioration de la survie globale à 12 mois pour les patients atteints d’un cancer du sang ayant reçu une allo-GCSH. L’essai, une étude internationale, multicentrique, randomisée, en double aveugle et contrôlée par placebo (NCT05762211), sera mené dans 59 sites d’investigation et devrait inclure 388 patients. Il s’agit, à ce jour, du plus grand essai contrôlé randomisé évaluant une thérapie à base de microbiote en oncologie.
Des études récentes mettent de plus en plus en exergue le rôle du microbiote intestinal, en établissant notamment un lien entre des altérations et des maladies telles que la sclérose latérale amyotrophique (SLA[8]). Le lien entre le microbiote intestinal et la SLA a été documenté, dans un premier temps, au travers de données précliniques, puis d’observations cliniques démontrant le rôle modificateur joué par le microbiote intestinal dans la maladie. À ce jour, il n’existe aucun traitement efficace contre la SLA, une maladie qui conduit au décès en moyenne dans les 3 à 5 ans après le diagnostic[9].
Depuis sa création, MaaT Pharma s’est engagée à rétablir la symbiose du microbiote dans les maladies graves avec des besoins médicaux non-satisfaits importants. De plus en plus d’études suggèrent que les patients atteints de SLA présentent une inflammation au niveau de l’intestin et des altérations de la composition des microbes intestinaux, avec des niveaux de bactéries bénéfiques réduits.
patients aux États-Unis et en Europe d’ici 2040
MaaT Pharma a ainsi décidé d’étendre sa recherche scientifique à la SLA, ce qui pourrait ouvrir la voie pour une approche dédiée pour plusieurs maladies neurodégénératives. La Société s’appuie sur le bon profil de sécurité de ses produits MET natifs (MaaT033/MaaT013), mais également sur les modes d’actions inhérents aux produits, à savoir la modulation immunitaire/les propriétés anti-inflammatoires et leur rôle central pour maintenir l’homéostasie.
Cette extension du portefeuille à une nouvelle indication souligne le potentiel de MaaT033 à être utilisé en tant que thérapie en utilisation seule ou adjuvante dans des situations aiguës ou chroniques.


This pipeline expansion to a new indication demonstrates the strong potential of MaaT033 to be used in acute or in chronic conditions as a standalone, adjunctive therapy.
ClinicalTrials.gov Identifier: NCT05889572
1 Castilla-Llorente. C, et al. Prognostic factors and outcomes of severe gastrointestinal GVHD after allogeneic hematopoietic cell transplantation. Bone Marrow Transplant. 2014 49(7):966-71. doi:10.1038/bmt.2014.69
2 Peled JU, et al. Role of the intestinal mucosa in acute gastrointestinal GVHD. Blood. 2016 128(20):2395-2402. doi: 10.1182/blood-2016-06-716738.
Staffas A, et al. The intestinal microbiota in allogeneic hematopoietic cell transplant and graft-versus-host disease. Blood. 2017 129(8):927-933. doi: 10.1182/blood-2016-09-691394. Erratum in: Blood. 2017 Apr 13;129(15):2204
Mathewson ND, et al. Gut microbiome-derived metabolites modulate intestinal epithelial cell damage and mitigate graft-versus-host disease. Nat Immunol. 2016 505-513. doi: 10.1038/ni.3400. Epub 2016 Mar 21. Erratum in: Nat Immunol. 2016 Sep 20;17 (10 ):1235.
3 Taur Y, et al. The effects of intestinal tract bacterial diversity on mortality following allogeneic hematopoietic stem cell transplantation. Blood. 2014 124(7):1174-82. doi:10.1182/blood-2014-02-554725.
Jenq RR, et al. Regulation of intestinal inflammation by microbiota following allogeneic bone marrow transplantation. J Exp Med. 2012 903-11. doi: 10.1084/jem.20112408.
4 Jenq RR, et al. Intestinal Blautia Is Associated with Reduced Death from Graft-versus-Host Disease. Biol Blood Marrow Transplant. 2015 1373-83. doi:10.1016/j.bbmt.2015.04.016.
Peled JU, et al. Intestinal Microbiota and Relapse After Hematopoietic-Cell Transplantation. J Clin Oncol. 2017 1650-1659. doi:10.1200/JCO.2016.70.3348
5 Global Data GVHD Epidemiology Report, Jan 2020.
6 EBMT data 2021
7 Malard, F., Vekhoff, A., Lapusan, S. et al. Gut microbiota diversity after autologous fecal microbiota transfer in acute myeloid leukemia patients. Nat Commun 12, 3084 (2021). https://doi.org/10.1038/s41467-021-23376-6
[8] Rowin et al., 2017; Nicholson et al, 2021; Blacher et al, 2019, Mazzini et al, 2020
[9] https://tousensellescontrelasla.fr/la-sla-cest-quoi/
[10] Yishan Ye, Wenjing Hao, Florent Malard, Mohamad Mohty, Emerging novel therapies for steroid-refractory acute graft-versus-host disease: recent advances and future directions, Current Opinion in Immunology, Volume 96, 2025, https://doi.org/10.1016/j.coi.2025.102649.
[11] Emmanuelle Godefroy, Frédéric Altare, Deciphering and harnessing gut microbiota–associated immune regulation in acute graft-versus-host disease, Current Opinion in Immunology, Volume 97, 2025, https://doi.org/10.1016/j.coi.2025.102676.
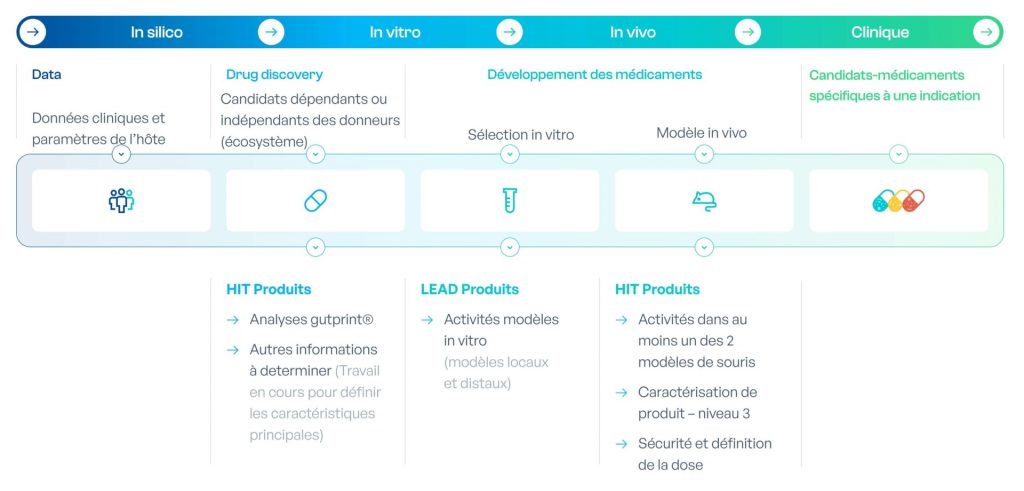
En utilisant notre plateforme d’analyse gutPrint, nous développons des produits dédiés pour chaque indication, qui combinent haute richesse et haute diversité bactérienne avec des réseaux fonctionnels bactériens spécifiques, dans le but d’améliorer le taux de réponse aux ICI. Chaque produit est conçu sur la base d’une analyse, effectuée par IA, de données issues de patients et de donneurs sains, et développé via notre technologie unique et innovante de co-culture, qui permet de répliquer et d’exploiter, à l’échelle industrielle, la richesse et la diversité de microbiote natifs. Cela nous permet d’adapter le produit à une composition spécifique pour une indication thérapeutique dédiée.
MaaT034, produit de co-culture « first-in-class », vise à optimiser les fonctions du microbiome intestinal avant et pendant l’immunothérapie dans les principales indications oncologiques, et à devenir une thérapie (néo)-adjuvante à travers les thérapies ICI, conduisant à une meilleure survie chez les patients atteints de cancer. L’objectif de MaaT Pharma est de développer MaaT034 en tant que thérapie en combinaison avec les ICI (c.-à-d. administration avant et en combinaison avec les ICI quel que soit le type de cancer) conduisant à de meilleurs résultats cliniques et à une incidence plus faible de complications que l’utilisation des ICI seuls.
Pour y parvenir, MaaT Pharma capitalisera sur les produits MET-N : un essai promu par les investigateurs est déjà en cours dans les tumeurs solides avec l’essai PICASSO (mélanome métastatique, avec Xervyteg® – MaaT013) pour évaluer la sécurité des produits MET-N en combinaison avec l’ICI et recueillir des données préliminaires d’efficacité évaluant l’impact des produits MET sur le système immunitaire et les réponses anti-tumorales.

MaaT03X est une thérapie issue de microbiote à écosystème complet super-compétent développée par co-culture adapté à des indications spécifiques. Grâce à la collecte de données auprès de patients, de donneurs sains et de la littérature, ainsi que de données recueillies au cours du développement de MaaT034 (échantillons fécaux et biologiques), MaaT Pharma alimente continuellement la plateforme d’IA gutPrint, pour développer des médicaments-microbiote de nouvelle génération

Sheri Simmons, Ph.D., est Directrice Scientifique par intérim au sein de MaaT Pharma. Sheri apporte une expertise approfondie en biotechnologie, en particulier dans le domaine du microbiome, ayant occupé des postes de direction scientifique chez Seres Therapeutics, au sein de l’équipe Microbiome Solutions de Johnson & Johnson, et plus récemment chez Seed Health, société leader dans le domaine des probiotiques. Dans ses fonctions, elle renforce le leadership scientifique de la Société, supervise les recherches précliniques, les initiatives en intelligence artificielle et data, et soutient les opérations liées à la demande d’Autorisation de Mise sur le Marché de Xervyteg® dans l’aGvH.
Sheri est titulaire d’un doctorat en océanographie biologique du Massachusetts Institute of Technology (MIT) et a obtenu un Bachelor of Arts (A.B.) en écologie et biologie évolutive à l’Université de Princeton, où elle a été diplômée summa cum laude, membre de Phi Beta Kappa, et lauréate de l’un des six prix récompensant les meilleures thèses de fin d’études en sciences.
Hervé Affagard is the CEO and co-founder of MaaT Pharma. For the past 15 years, Hervé has been an intra/entrepreneur in the healthcare industry, after starting his career in IT in the steel industry. In late 2014, Hervé co-founded the company alongside Dr. Joël Doré, author of nearly 500 publications, and
one of the world’s most cited authors in the microbiome sphere today, after a professional career that spanned multiple industries. Hervé has led MaaT Pharma’s development from its early concept in 2013 and has been at the forefront of the development of the microbiome healthcare ecosystem in France and Europe. In January 2022, Hervé has been elected President of Allliance Promotion Microbiote, an organization founded in 2021 to support the microbiome sector development in France.
Engineer, MBA