MaaT013 (Xervyteg®) : Résultats positifs de l'étude pivotale dans la maladie aiguë du greffon contre l’hôte
Design de l'étude
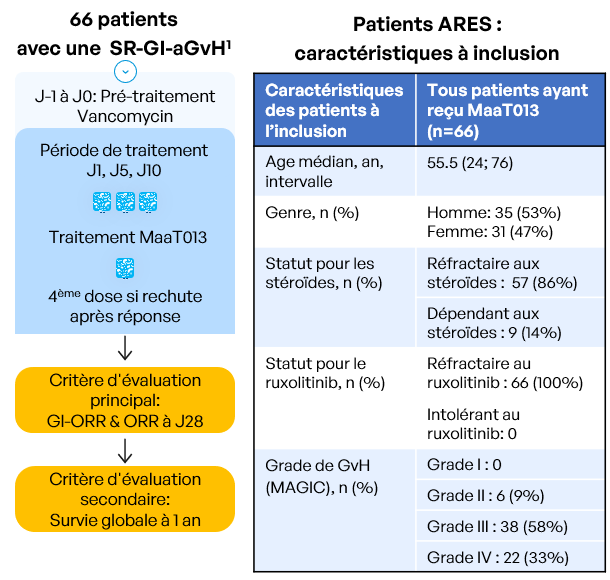
Critères d’inclusion:
- Âge ≥ 18 ans
- Allo-GCSH avec tout type de donneur, source de cellules souches, prophylaxie de la GvH ou schéma de conditionnement
- Patients développant un épisode d’aGvH avec atteinte gastro-intestinale selon les directives MAGIC (grades II à IV), avec ou sans atteinte d’autres organes (Harris et al., 2016)
- Patients résistants aux corticoïdes ET soit résistants à OU intolérants au ruxolitinib (patients intolérants : ayant présenté un événement indésirable de grade 3 ou plus, apparu sous traitement et attribué au ruxolitinib, qui n’a pas été résolu dans les 7 jours suivant l’arrêt du ruxolitinib). Le diagnostic doit être confirmé dans les 48 heures précédant le début du pré-traitement de l’étude.
L’étude a été menée dans 6 pays européens (Autriche, Belgique, France, Allemagne, Italie et Espagne) sur 50 sites.
ARES : Forte réponse à MaaT013 (Xervyteg®) dans l’aGvH après un échec des traitements aux corticoïdes et au ruxolitinib
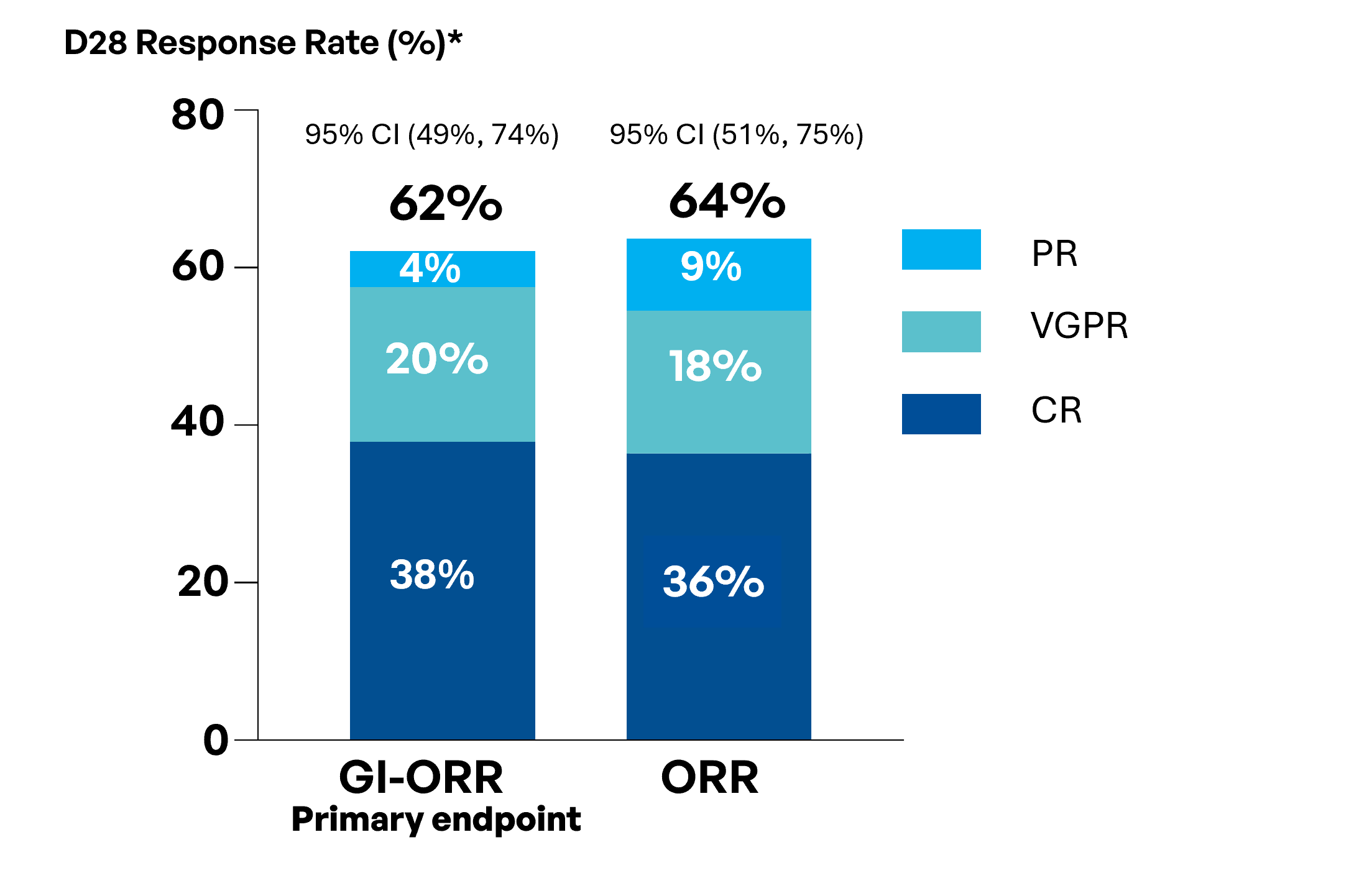
-
62 % de GI-ORR avec des taux élevés de réponse complète et de très bonne réponse partielle.
-
64% de ORR indiquant une efficacité au-delà du tractus gastro-intestinal.
- Jour 56 : Efficacité durable avec un GI-ORR de 47% et un ORR tous organes de 45 %.
- Mois 3 : le GI-ORR et l’ORR tous organes sont tous deux à 44%, confirmant une réponse soutenue.
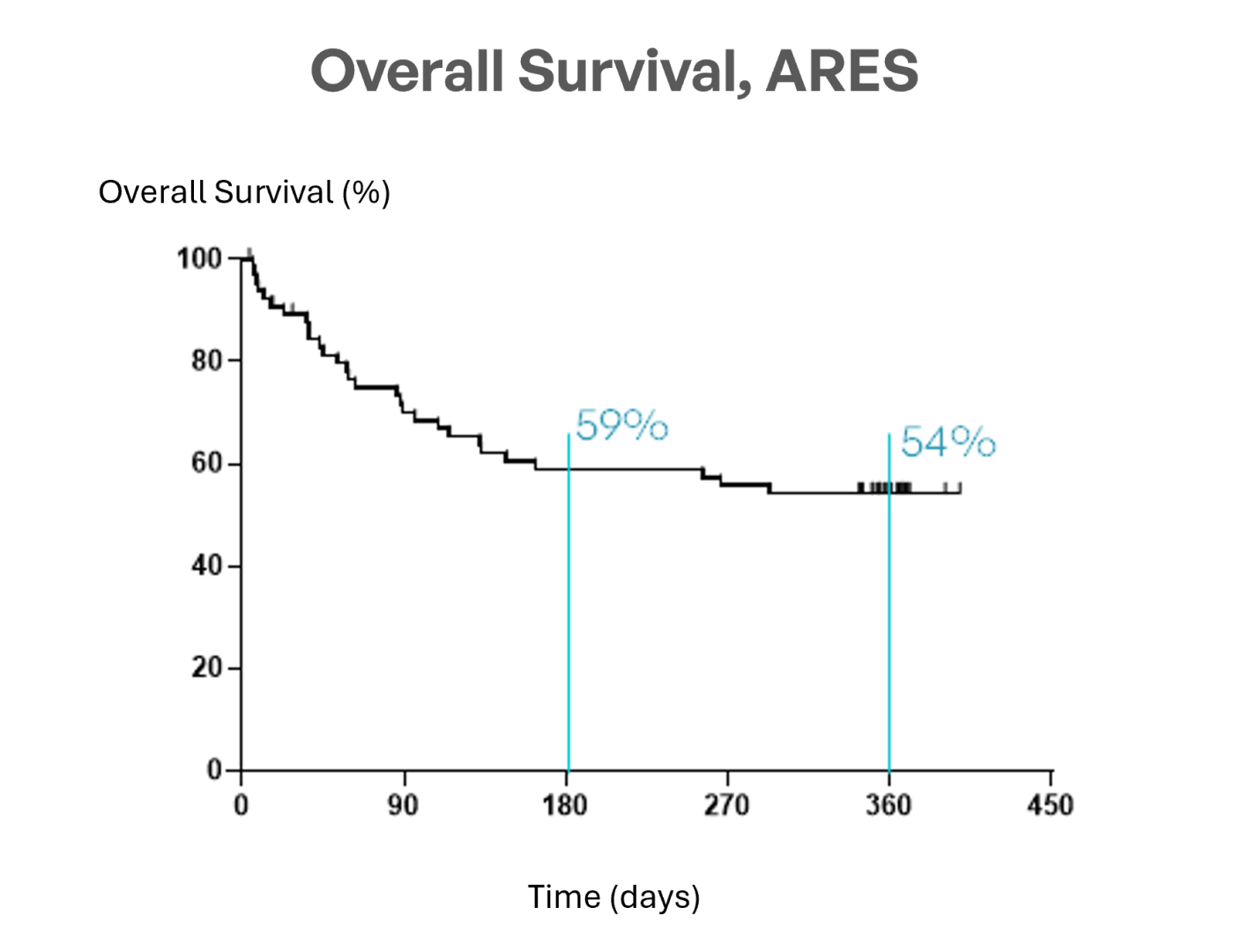
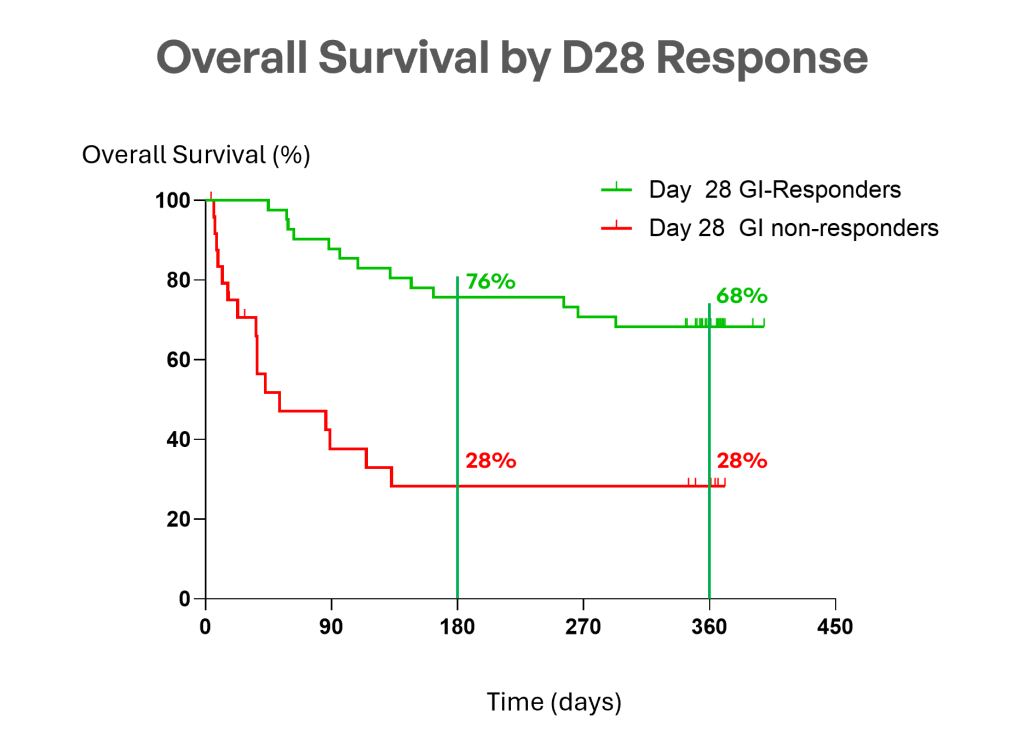
MaaT013 (Xervyteg®) affiche un taux de survie globale à un an de 54%, dépassant les attentes, tandis que la cohorte européenne CHRONOS1, menée à la même période dans des centres participant également à l’étude ARES et selon des critères de sélection harmonisés, a rapporté un taux de survie de 29 % lors du congrès de l’EBMT 2026 et dans un article publié dans la revue BMT, compte tenu des limites inhérentes à sa conception rétrospective.
1: essai de 3e ligne avec critères d’éligibilité harmonisés. Étude non randomisée, sans appariement ; à caractère purement descriptif – ÉTUDE CHRONOS – Clausen et al., BMT 2026
“ Ces résultats confirment que MaaT013 apporte un bénéfice clinique durable chez les patients atteints de GI-aGvHD. L’obtention d’un GI-ORR de 62 % au jour 28, le maintien des réponses dans le temps et l’atteinte d’une survie globale à un an de 54 % constituent une avancée significative pour répondre à ce besoin médical critique non satisfait. ”
Dr. Malard, professeur d’hématologie à l’hôpital Saint-Antoine et à Sorbonne Université, investigateur principal de l’essai pivotal ARES

📰 MaaT013 (Xervyteg®) fait actuellement l’objet d’une évaluation par l’Agence européenne des médicaments (EMA) suite au dépôt, en juin, d’une demande d’autorisation de mise sur le marché pour le traitement des patients adultes atteints d’aGvH, y compris avec atteinte gastro-intestinale, ayant déjà reçu deux lignes de traitement.
- 1Dans l’étude ARES, la SR-GI-aGvHD est définie comme les patients résistants aux corticoïdes ET résistants OU intolérants au ruxolitinib (patients intolérants : ayant présenté un effet indésirable de grade 3 ou plus, apparu sous traitement et attribué au ruxolitinib, qui ne s’est pas résolu dans les 7 jours suivant l’arrêt du ruxolitinib). Les cas de SR-aGvHD incluent les patients ayant reçu une forte dose de corticoïdes systémiques (méthylprednisolone 2 mg/kg/jour – ou une dose équivalente de prednisone 2,5 mg/kg/jour), administrée seule ou en association avec un inhibiteur de la calcineurine ou un inhibiteur de mTOR, et qui ont présenté l’une ou l’autre des caractéristiques suivantes :
- Absence d’amélioration (c’est-à-dire pas de diminution du stade dans au moins 1 organe impliqué) après ≥ 5 jours de traitement par corticoïdes à une dose équivalente à 2 mg/kg/j de méthylprednisolone, ou
- Progression (c’est-à-dire augmentation dans un organe ou atteinte d’un nouvel organe) après ≥ 3 jours de traitement par corticoïdes à une dose équivalente à 2 mg/kg/j de méthylprednisolone, ou
- Les patients traités par 1 mg/kg/j de corticoïdes parce que le médecin a estimé qu’ils ne toléreraient pas 2 mg/kg/j et qui correspondent à la définition des patients SR, ou
- Les patients qui ont commencé un traitement par corticoïdes à une dose plus faible (au moins 1 mg/kg/j d’équivalent méthylprednisolone) mais qui développent des nouveaux symptômes dans un autre organe,ou
- Les patients qui ne peuvent pas tolérer la diminution progressive des corticoïdes, c’est-à-dire qui commencent les corticoïdes à 2,0 mg/kg/j, montrent une réponse, mais progressent avant qu’une diminution de 50 % de la dose initiale de corticoïdes ne soit atteinte.
- La résistance au ruxolitinib est définie comme l’un des éléments suivants (Mohty M. 2020):
- Progression de la GvHD par rapport à l’état initial après au moins 5 jours de traitement par ruxolitinib, basée soit sur une augmentation objective du stade/grade, soit sur une atteinte d’un nouvel organe, ou
- Absence d’amélioration de la GvHD (au moins une réponse partielle) par rapport à l’état initial, après au moins 14 jours de traitement par ruxolitinib, ou
- Perte de réponse, définie comme une aggravation objective de la GvHD déterminée par une augmentation du stade, du grade ou l’atteinte d’un nouvel organe, à tout moment après une amélioration initiale, ou
- Absence de réponse complète ou de très bonne réponse partielle au 28ème jour après le début du traitement avec ruxolitinib.
- L’intolérance au ruxolitinib est définie comme des manifestations de GvHD persistant sans amélioration chez les patients ayant présenté un effet indésirable de grade 3 ou plus, apparu sous traitement et attribué au ruxolitinib, qui ne s’est pas résolu dans les 7 jours suivant l’arrêt du ruxolitinib.
- aGVHD : maladie aiguë du greffon contre l’hôte
- GI : gastro-intestinal
- MAGIC : Consortium international Mount Sinai pour la GVHD aiguë
- ORR : taux de réponse global
- SR : réfractaire aux stéroïdes
- D : Jour
- M : Mois

